Bufory i roztwory
Roztwory buforowe – stabilizacja pH w analizie laboratoryjnej
Roztwory buforowe to niezbędny element pracy w nowoczesnym laboratorium, szczególnie tam, gdzie kontrola pH buforu ma kluczowe znaczenie dla przebiegu reakcji chemicznych i biologicznych. Każdy roztwór buforowy umożliwia utrzymanie względnie stałego odczynu nawet przy dodatku niewielkich ilości kwasów, zasad lub podczas rozcieńczania.
Dzięki temu bufory pH są szeroko wykorzystywane w analizie chemicznej, farmacji, biotechnologii oraz w procesach przemysłowych związanych z kontrolą jakości i badaniami właściwości substancji.
Fizykochemiczne podstawy działania układów buforujących
Podstawowa definicja roztworu buforowego opiera się na obecności pary sprzężonej: słabego kwasu i jego soli lub słabej zasady i jej soli. Klasyczna definicja roztworu buforowego wskazuje, że układ taki przeciwdziała zmianom pH poprzez reakcje neutralizacji.
Przykładowo:
- bufor kwasowy:
CH₃COOH + CH₃COONa - bufor zasadowy:
NH₃ + NH₄Cl
Reakcje odpowiedzialne za stabilizację pH roztworu buforowego:
- neutralizacja jonów H⁺:
CH₃COO⁻ + H⁺ → CH₃COOH - neutralizacja jonów OH⁻:
CH₃COOH + OH⁻ → CH₃COO⁻ + H₂O
Opis ilościowy zapewnia równanie Hendersona-Hasselbalcha: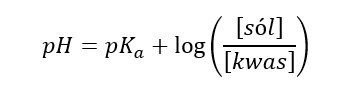
To właśnie te zależności pozwalają precyzyjnie określić pH buforu i jego zakres działania.
Rola układów buforujących w fizjologii i farmakologii
Roztwory buforowe pH odgrywają istotną rolę nie tylko w chemii, ale również w układach biologicznych. W organizmach żywych odpowiadają za utrzymanie stabilnego środowiska reakcji enzymatycznych, gdzie nawet niewielka zmiana pH roztworu buforowego może zaburzyć funkcjonowanie białek.
W farmacji bufory pH stosuje się w formulacjach leków, aby zapewnić ich trwałość i bezpieczeństwo. W przemyśle spożywczym oraz kosmetycznym roztwory buforowe stabilizują właściwości produktów końcowych.
Optymalizacja i stabilizacja parametrów w warunkach laboratoryjnych
W praktyce laboratoryjnej przygotowanie odpowiedniego roztworu buforowego wymaga precyzji oraz kontroli parametrów. Warto korzystać z narzędzi takich jak mierniki laboratoryjne, w tym pH metry przenośne i pH metry stacjonarne, które umożliwiają dokładny pomiar pH buforu. W bardziej zaawansowanych analizach wykorzystuje się również tlenomierze.
Proces przygotowania roztworu buforowego:
- dobór układu buforującego (najlepiej z użyciem kalkulatora buforów)
- rozpuszczenie składników w około 80–90% docelowej objętości wody
- dokładne wymieszanie i pomiar pH
- korekta pH przy użyciu 0,1–1 M HCl lub NaOH
- uzupełnienie objętości w kolbie miarowej do wartości końcowej
Tak przygotowane roztwory buforowe zapewniają stabilność i powtarzalność wyników w analizach laboratoryjnych.
Specyfika i zakresy robocze wybranych mieszanin analitycznych
Dobór odpowiednich buforów pH zależy od wymaganego zakresu działania. Różne roztwory buforowe pH pracują efektywnie w określonych przedziałach:
- pH 2–3: bufor ftalanowy
- pH 4–5: bufor octanowy (CH₃COOH + CH₃COONa)
- pH 6–8: bufor fosforanowy (NaH₂PO₄ / Na₂HPO₄ – układ wodorosoli)
- pH 7–8: HEPES (biochemia)
- pH 8–9: TAE (Tris-octan-EDTA)
- pH 9–10: bufor boranowy
- pH >10: bufor węglanowy
Każdy taki roztwór buforowy charakteryzuje się określoną pojemnością buforową i zakresem działania, zwykle ±1 jednostki pH względem wartości pKa.
Dzięki właściwemu doborowi i przygotowaniu roztworów buforowych możliwe jest utrzymanie stabilnych warunków reakcji, co ma kluczowe znaczenie w nowoczesnych badaniach właściwości oraz analizach chemicznych i biologicznych.






