Elektroliza wody
Elektroliza wody – czym jest i na czym polega?
Elektroliza wody to proces chemiczny, w którym woda jest rozkładana na wodór i tlen przy użyciu prądu elektrycznego. Jest to jedna z podstawowych metod pozyskiwania wodoru, który może być wykorzystany jako ekologiczne paliwo. Elektroliza wody znajduje zastosowanie w przemyśle chemicznym, energetyce oraz badaniach naukowych.
Co to jest elektroliza wody?
Elektroliza wody to proces elektrochemiczny polegający na przepuszczaniu prądu przez wodny roztwór elektrolitu w celu rozbicia cząsteczek wody na tlen i wodór. Prąd elektryczny inicjuje reakcje chemiczne, które prowadzą do wydzielania gazów na elektrodach. Jest to proces odwrotny do reakcji spalania wodoru.
Reakcja elektrolizy wody.
Podstawowa reakcja elektrolizy wody przebiega zgodnie z poniższymi równaniami elektrochemicznymi:
Na katodzie (redukcja):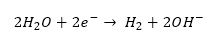
Na anodzie (utlenianie):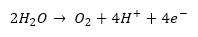
Całkowita reakcja elektrolizy wody: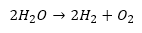
Proces ten wymaga dostarczenia energii elektrycznej, zazwyczaj pochodzącej z odnawialnych z źródeł energii, takich jak energia słoneczna czy wiatrowa.
Elektroliza wody metody.
Istnieje kilka metod elektrolizy wody, w tym:
- Alkaliczna elektroliza wody (AWE) – wykorzystuje roztwory wodorotlenku sodu lub potasu jako elektrolit.
- Elektroliza membranowa (PEM) – stosuje membrany polimerowe jako elektrolit, co zwiększa efektywność procesu.
- Elektroliza wysokotemperaturowa (SOEC) – przeprowadzona w wysokich temperaturach, co zmniejsza zużycie energii elektrycznej.
Każda z tych metod ma swoje zalety i znajduje zastosowanie w różnych sektorach przemysłu.
Elektroliza wody co się wytrąca.
Podczas elektrolizy wody na elektrodach wytrącają się gazy:
- Na katodzie wydziela się wodór (H2), który można wykorzystywać jako paliwo lub surowiec chemiczny.
- Na anodzie powstaje tlen (O2), który może być stosowany w przemyśle lub medycynie.
W zależności od użytego elektrolitu, mogą również powstawać inne produkty, takie jak jony hydroksylowe (OH-) czy jony wodorowe (H+), które wpływają na pH roztworu.
Elektroliza wody to ważny proces technologiczny o szerokim zastosowaniu w przemyśle i energetyce, szczególnie w kontekście rozwoju zielonej energii i produkcji paliwa wodorowego.
Zapraszamy do zapoznania się z naszą ofertą handlową, w sprzedaży posiadamy urządzenia chłodnicze, grzewcze, szkło laboratoryjne oraz elektrody i czujniki.
